
6. pH van een oplossing van een sterk zuur
Als het sterke zuur HCl opgelost wordt in water, zullen bijna alle HCl-moleculen een proton afgeven:
HCl(aq) + H2O(vl) 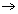 H3O+(aq) + Cl-(aq)
H3O+(aq) + Cl-(aq)
of
HCl(aq) 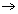 H+(aq) + Cl-(aq)
H+(aq) + Cl-(aq)
Daardoor zal [H3O+] of [H+] gelijk zijn aan de oorspronkelijke concentratie van het zuur HCl:
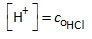
Voorbeeld: 0.1 mol/L HCl(aq) 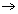 [H+] = 0,1 mol/L
[H+] = 0,1 mol/L 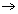 pH = -log 0,1 = 1.
pH = -log 0,1 = 1.
pH + pOH = 14 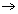 pOH = 13.
pOH = 13.
In dit geval is de concentratie van de waterstofionen afkomstig van het water te verwaarlozen naast de 0,1 mol/L afkomstig van de ionisatie van HCl. In zuiver water is die concentratie slechts 10-7 mol/L. Door de aanwezigheid van een overvloed aan waterstofionen afkomstig van het sterke zuur HCl, zal het waterevenwicht helemaal naar links schuiven (Le Chatelier).
Samengevat
|
pH van een oplossing van een sterk zuur in water
|
[H+] = coHA
Bereken hieruit de pH
|