
Een waterstofchloridemolecule is een dipoolmolecule. Door interactie met de watermoleculen (ook dipoolmoleculen) kunnen de HCl-moleculen gemakkelijk tussen de watermoleculen bewegen.
Het feit dat de oplossing van HCl in water de stroom geleidt, wijst erop dat er nog meer aan de hand is. Er blijken immers ionen aanwezig te zijn die verantwoordelijk zijn voor de elektrische geleiding. Die ionen zijn ontstaan doordat de HCl-moleculen niet enkel oplossen in het water, maar daarbij ook ionen vormen.
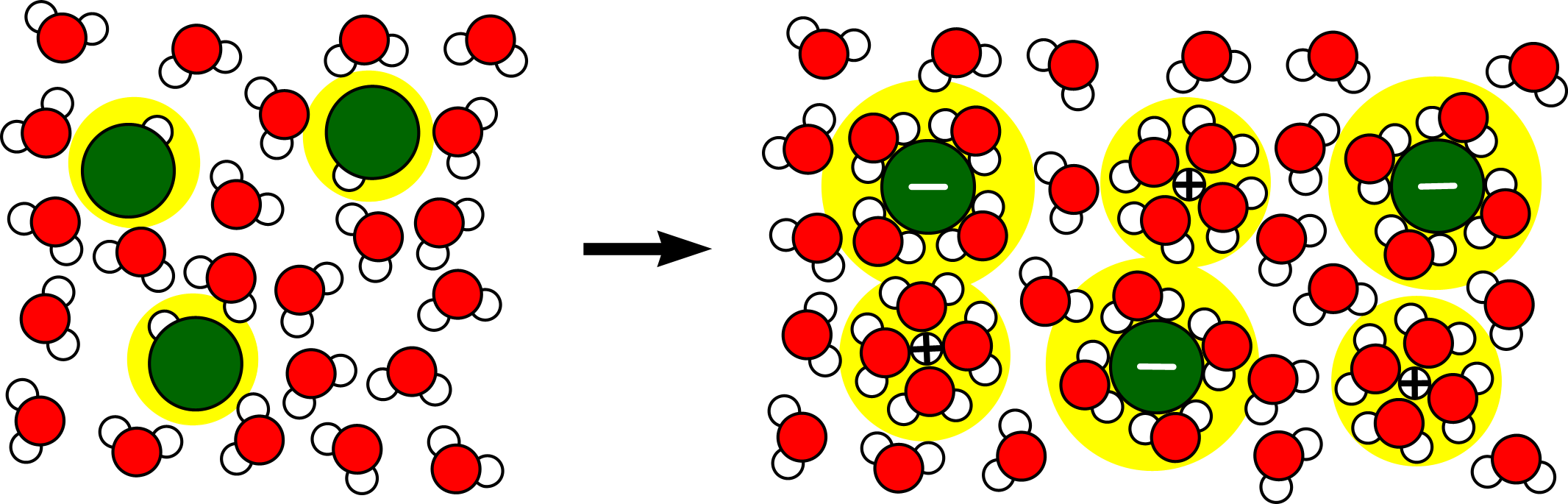
HCl(aq) 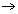 H+(aq) + Cl−(aq)
H+(aq) + Cl−(aq)
De vorming van ionen noemt men ionisatie.
De oplossing van waterstofchloride bevat uiteindelijk gehydrateerde waterstof- en chloride-ionen: H+(aq) en Cl-(aq).
Samengevat
Ionisatie van covalente verbindingen |
Sommige polaire stoffen lossen niet enkel op in water, maar vormen daarbij ionen (ionisatie).
Door het feit dat er daarbij ionen ontstaan, geleidt de oplossing de stroom.
Dergelijke stoffen noemen we daarom ook elektrolyten.
Elektrolyten zijn samengestelde stoffen die de stroom geleiden na smelten of oplossen in water.
|