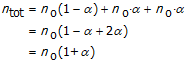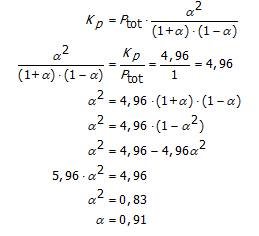Gegeven de evenwichtsreactie
PCl5(g) ⇌ PCl3(g) + Cl2(g)
in een gesloten vat met constant volume bij 556 K.
no is het oorspronkelijk aantal mol PCl5 en a is de fractie van de PCl5-moleculen dat gedissocieerd is in PCl3 en Cl2.
Leid een uitdrukking af voor Kp in functie van a en de totale evenwichtsdruk P.
Als Kp = 4,96 en P = 1 bar, bereken a.
Stel een tabel op waarin een overzicht gegeven wordt van de hoeveelheden die aanwezig zijn vóór de reactie,
de hoeveelheden die verdwijnen en ontstaan tijdens de reactie en de hoeveelheden bij evenwicht.
Bereken het totaal aantal mol bij evenwicht.
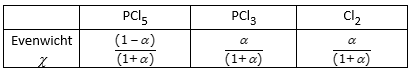
Bereken de molfracties van de componenten bij evenwicht.
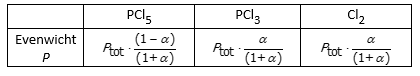
Bereken nu de partieeldrukken als Ptot de totaaldruk voorstelt.
Vervang de partieeldrukken in de Kp door deze waarden.
Bereken a als Kp = 4,96 en Ptot = 1 bar.

![]()