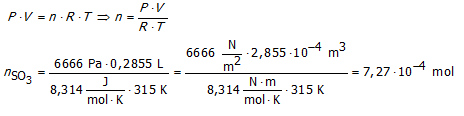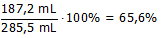Beschouw de volgende reactie:
2 SO2(g) + O2(g)  2 SO3(g)
2 SO3(g)
a. Wanneer men 285,5 mL SO2 laat reageren met 158,9 mL O2 (beide volumes gemeten bij 315 K en 6666 Pa),
wat is het beperkend reagens en de theoretische opbrengst van SO3?
b. Wanneer 187,2 mL SO3 wordt opgevangen (bij 315 K en 6666 Pa) wat is het rendement van de reactie?
ALLE gasvolumes werden gemeten bij dezelfde temperatuur (315 K) en dezelfde druk (6666 Pa).
Deze volumes zijn dus rechtevenredig met het aantal mol.
a
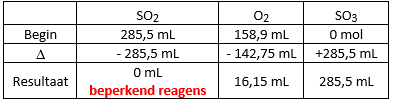
Bepaal het beperkend reagens en de theoretische opbrengst van SO3.
Dit kan je best bepalen uit een tabel waarin een overzicht gegeven wordt van de hoeveelheden die aanwezig zijn vóór de reactie,
de hoeveelheden die verdwijnen en ontstaan tijdens de reactie en de hoeveelheden na de reactie.
Wat is de theoretische opbrengst van SO3?
b
Wanneer 187,2 mL SO3 wordt opgevangen (bij 315 K en 6666 Pa) wat is het rendement van de reactie?

![]()
 2 SO3(g)
2 SO3(g)