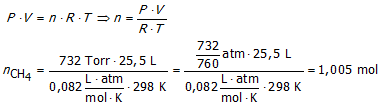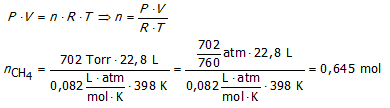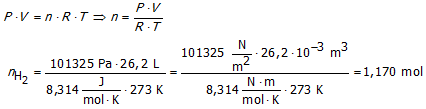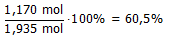![]()
Waterstofgas (een mogelijk brandstofgas) kan worden gevormd door de reactie van methaangas (CH4) met water volgens:
CH4(g) + H2O(g)  CO(g) + 3 H2(g)
CO(g) + 3 H2(g)
In een specifieke reactie wordt 25,5 L methaangas (gemeten bij een druk van 732 Torr en 25 °C) gemengd met 22,8 L waterdamp (gemeten bij 702 Torr en 125 °C).
Tijdens de reactie worden 26,2 L H2 gevormd, gemeten bij standaardomstandigheden.
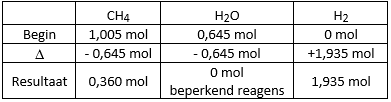
Wat is het rendement van de reactie?