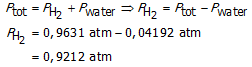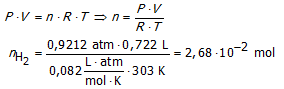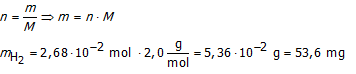![]()
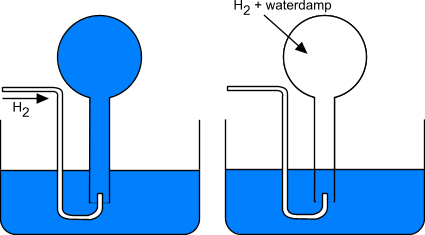
| Waterstofgas, gevormd tijdens een chemische reactie, wordt opgevangen onder water. De totaaldruk is 0,9631 atm bij 30°C. Wat is de partieeldruk van het waterstofgas dat wordt opgevangen (de dampdruk van water is 0,041 92 atm bij deze temperatuur). Wanneer het totaal volume gas dat wordt opgevangen gelijk is aan 0,722 L, wat is de massa van het gevormde H2? |
 |