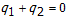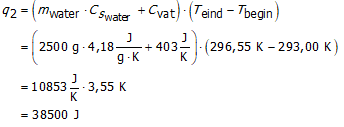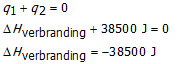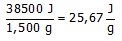![]()
1,500 g van een koolwaterstofbrandstof wordt in een bomcalorimeter gebracht met een overmaat aan O2.
De calorimeter is gevuld met 2,500 L water.
De begintemperatuur bedraagt 20,00 °C.
Na de verbranding bedraagt de eindtemperatuur 23,55 °C.
Bereken de reactiewarmte per gram brandstof.
Warmtecapaciteit van de calorimeter zonder het water is 403 J.K−1.