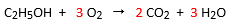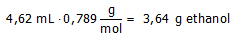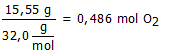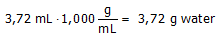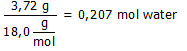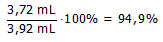De verbranding van vloeibare ethanol (C2H5OH) leidt tot de vorming van koolstofdioxide en water.
Nadat 4,62 mL ethanol (ρethanol=0,789 g/mL) werd verbrand in de aanwezigheid van 15,55 g zuurstofgas werd 3,72 mL water gevormd (ρwater=1,000 g/mL).
Bepaal het beperkend reagens, de theoretische en de procentuele opbrengst.
Schrijf eerst de reactievergelijking.
Wat is de massa van 4,62 mL ethanol?
Hoeveel mol ethanol is dit?
Hoeveel mol is 15,55 g O2?
Wat is de massa van 3,72 mL water?
Hoeveel mol water is dit?
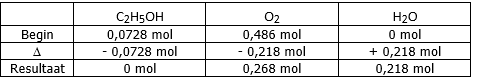
De theoretische opbrengst kan je best bepalen uit een tabel waarin een overzicht gegeven wordt van
de hoeveelheden die aanwezig zijn vóór de reactie, de hoeveelheden die verdwijnen en ontstaan
en de hoeveelheden na de reactie.
Wat is het beperkend reagens?
Wat is de theoretische opbrengst (H2O) in mL?
Hoe groot is het rendement van de reactie?

![]()