L-carnosine ( = b-alanyl-L-histidine , C9H14O3N4, M = 226,23 g/mol) is een veel gebruikt voedingssupplement: het zou het verouderingsproces tegengaan (anti-oxiderend), het zou zelfs de sexuele potentie verhogen.
In zijn meest basische vorm is het een zwakke base (B-) die stapsgewijs maximaal 3 H+ kan opnemen bij neutralisatie met een zuur.
Dit product is ook in biochemische laboratoria te synthetiseren en wordt na omkristallisatie bekomen in de vorm van het zwitterion HB .
Een stockoplossing van dit zwitterion in water heeft een pH van 8,06.
40,0 mL van deze stockoplossing wordt getitreerd met 0,100 mol/L NaOH(aq) en het SP wordt bereikt na toevoegen van 8,10 mL NaOH(aq).
40,0 mL van dezelfde stockoplossing wordt ook getitreerd met 0,150 mol/L HCl(aq) en het SP1 wordt bereikt na toevoegen van 5,40 mL HCl(aq).
Na toevoegen van 4,00 mL HCl(aq) bedroeg de pH 6,30 en na toevoegen van 8,00 mL HCl(aq) bedroeg de pH van de oplossing 2,52.
a. Bereken de concentratie van het zwitterion van L-carnosine in de stockoplossing.
b. Bereken pKb1 , pKb2 en pKb3 van L-carnosine.
c. Bereken de pH bij het SP in de NaOH-titratie.
d. Bereken de pH bij het SP1 in de HCl-titratie.
e. Hoeveel mL 0,150 mol/L HCl(aq) moet men bij 40,0 mL van de zwitterion-oplossing toevoegen om de fysiologische pH van 7,10 te bekomen?
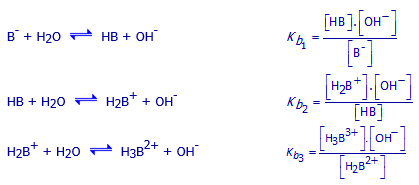
De meest basische vorm van L-carnosine (B-) is een zwakke base die, stapsgewijs, 3 protonen kan opnemen. Schrijf de 3 hydrolysereacties met de uitdrukkingen voor de drie baseconstanten.
a. Bereken de concentratie van het zwitterion van L-carnosine in de stockoplossing.
40,0 mL van de stockoplossing
van HB wordt getitreerd met 0,100 mol/L NaOH(aq) en het SP wordt
bereikt na toevoegen van 8,10 mL NaOH(aq).
Bereken hieruit de concentratie van HB.
40,0 mL van dezelfde
stockoplossing wordt ook getitreerd met 0,150 mol/L HCl(aq) en
het SP1 wordt bereikt na toevoegen van 5,40 mL HCl(aq).
Ook hieruit kan je de concentratie van HB berekenen.
b. Bereken pKb1 , pKb2 en pKb3 van L-carnosine.
40,0 mL van dezelfde stockoplossing
wordt ook getitreerd met 0,150 mol/L HCl(aq) en het SP1 wordt bereikt na toevoegen van 5,40 mL HCl(aq). Na
toevoegen van 4,00 mL HCl(aq) bedroeg de pH 6,30 en na toevoegen van 8,00 mL HCl(aq) bedroeg de pH van de
oplossing 2,52.
Bereken uit deze gegevens pKb2
40,0 mL van dezelfde
stockoplossing wordt ook getitreerd met 0,150 mol/L HCl(aq) en
het SP1 wordt bereikt na toevoegen van 5,40 mL HCl(aq).
Na toevoegen van 4,00 mL HCl(aq) bedroeg de pH 6,30 en na
toevoegen van 8,00 mL HCl(aq) bedroeg de pH van de oplossing
2,52.
Bereken uit deze gegevens pKb3.
Een stockoplossing
van dit zwitterion in water heeft een pH van 8,06.
Bereken uit deze gegevens pKb1.
c. Bereken de pH bij het SP in de NaOH-titratie.
40,0 mL van de stockoplossing
van HB wordt getitreerd met 0,100 mol/L NaOH(aq) en het SP wordt
bereikt na toevoegen van 8,10 mL NaOH(aq).
Bereken uit deze gegevens de pH bij het SP van de NaOH-titratie.
d. Bereken de pH bij het SP1 in de HCl-titratie.
40,0 mL van de stockoplossing
wordt getitreerd met 0,150 mol/L HCl(aq) en het SP1 wordt bereikt na toevoegen van 5,40 mL HCl(aq).
Bereken uit deze gegevens de pH bij het SP1 van de HCl-titratie.
e. Hoeveel mL 0,150 mol/L HCl(aq) moet men bij 40,0 mL van de zwitterion-oplossing toevoegen om de fysiologische pH van 7,10 te bekomen?
De stockoplossing van het zwitterion bevat een amfolyt en heeft een pH = 8,06 (Gegeven).
Bij toevoegen van HCl wordt HB progressief omgezet in H2B+. Tijdens die omzetting hebben we te maken met een buffer H2B+ / HB. Bij het eerste SP is alle HB omgezet in H2B+: een amfolyt met pH = 4,63 (§ d). De pH van 7,10 ligt dus in dit buffergebied.
Bereken met deze gegevens hoeveel ml HCl-oplossing moet toegevoegd worden opdat de pH van de buffer 7,10 zou bedragen.

![]()