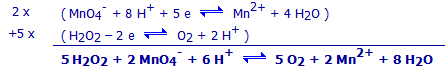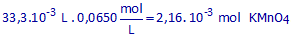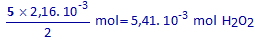1,24 g onzuiver BaO2 (bariumperoxide) wordt opgelost in zuur midden (H+) waarbij H2O2(aq) geproduceerd wordt.
Dit laatste wordt getitreerd met een 0,0650 mol/L KMnO4-oplossing, waarbij MnO4- gereduceerd wordt tot Mn2+ en
H2O2 geoxideerd wordt tot O2(g).
Het SP ligt bij 33,3 mL.
Hoeveel massa% BaO2 bevat het monster?
Schrijf de reactie die plaatsheeft bij oplossen van BaO2 in zuur midden.
In welke stof wordt BaO2 omgezet? Hoeveel van die stof ontstaat er daarbij?
Schrijf de reactie (deelreacties + totaalreactie) die optreedt tijdens het titreren van de H2O2–oplossing met KMnO4.
Hoeveel KMnO4 is er aanwezig in 33,3 mL 0,0650 mol/L KMnO4-oplossing?
In welke verhouding reageren H2O2 en KMnO4 met elkaar?
Hoeveel H2O2 reageert er met 2,16.10-3 mol KMnO4?
Hoeveel mol BaO2 was er dus in het monster aanwezig? Hoeveel gram is dit? Hoeveel massa%?

![]()